Змішана гіперліпідемія характеризується підвищеним рівнем ліпопротеїнів низької щільності (ЛПНЩ) та ліпопротеїнів, багатих на тригліцериди, у плазмі крові, що призводить до підвищеного ризику атеросклеротичних серцево-судинних захворювань у цій групі пацієнтів.
ANGPTL3 пригнічує ліпопротеїнліпазу та ендосепіазу, а також поглинання печінкою ліпопротеїнів, багатих на тригліцериди. Носії інактивованого варіанту ANGPTL3 мали нижчі рівні тригліцеридів, холестерину ЛПНЩ, холестерину ліпопротеїнів високої щільності (ЛПВЩ) та холестерину, що не належить до ЛПВЩ, а також нижчий ризик атеросклеротичних серцево-судинних захворювань. Зодасіран – це препарат на основі малої інтерферуючої РНК (РНК-інтерференції), який впливає на експресію ANGPTL3 у печінці.
Змішана гіперліпідемія стосується підвищеного рівня холестерину ліпопротеїнів низької щільності (ЛПНЩ) та ліпопротеїнів, багатих на тригліцериди. Ліпопротеїни, багаті на тригліцериди (включаючи хіломікрони, ліпопротеїни дуже низької щільності (ЛПДНЩ) та залишковий холестерин), відіграють важливу роль у розвитку атеросклеротичного захворювання. Ефективного лікування змішаної гіперліпідемії не існує.
Відомо, що препарати Бейтса знижують рівень тригліцеридів (ТГ), але це зниження обмежене. Водночас препарати, що знижують рівень ТГ, включаючи препарати Бейтса (такі як ейкозапентаєнова оцтова кислота тощо), не мають суттєвого впливу на ризик атеросклеротичного захворювання, спричиненого підвищеним рівнем залишкового холестерину. Крім того, попередні дослідження пацієнтів, які вже приймають статини, показали, що комбіновані препарати, що знижують рівень ТГ, не знижують ризик серцево-судинних подій. Ці фактори дуже ускладнюють лікування змішаної гіперліпідемії.
ANGPTL3 (ангіопоетиноподібний білок 3) регулює метаболізм ліпідів та ліпопротеїнів, включаючи тригліцериди та холестерин невисокої щільності (ЛПВЩ), шляхом зворотного пригнічення поглинання печінковими ліпопротеїнліпазами, ендосепіазами та рецепторами ліпопротеїнів низької щільності (ЛПНЩ). Було виявлено, що варіант інактивації ANGPTL3 призводить до підвищеної активності ліпопротеїнліпази та ендосепіази, що, у свою чергу, призводить до низького рівня ліпопротеїнів у плазмі крові у більшості випадків. До них належать ліпопротеїни, багаті на тригліцериди (тобто хіломікрони, залишковий холестерин, ЛПДНЩ, ліпопротеїни середньої щільності [ЛПСЩ]), ЛПНЩ, ліпопротеїни високої щільності (ЛПВЩ), ліпопротеїн (а) та їх холестеринові компоненти. Гетерозиготні люди, які є носіями цього варіанту, мають приблизно на 40% знижений ризик атеросклеротичного захворювання, і жодного несприятливого клінічного фенотипу не виявлено. ANGPTL3 експресується в печінці, а терапії пригнічення генів, спрямовані на його мРНК, відомі як препарати на основі малих інтерферуючих РНК (siRNA), є перспективним гібридним методом лікування гіперліпідемії.
12 вересня 2024 року в журналі «New England Journal of Medicine» (NEJM) було опубліковано дослідження ARCHES 2, яке підтверджує, що препарат siRNA зодасиран значно знижує рівень тригліцеридів у пацієнтів зі змішаною гіперліпідемією [1]. ARCHES-2 – це подвійне сліпе, плацебо-контрольоване дослідження фази 2b з вивченням діапазону доз. У дослідженні взяли участь 204 пацієнти зі змішаною гіперліпідемією (рівень тригліцеридів натщесерце 150-499 мг/дл, рівень холестерину ЛПНЩ ≥70 мг/дл або рівень холестерину не-ЛПВЩ ≥100 мг/дл). Їх розділили на групи зодасирана 50 мг, 100 мг, 200 мг та контрольну групу плацебо. Пацієнти отримували підшкірні ін'єкції на 1-му та 12-му тижні та отримували подальшу профілактику до 36-го тижня.
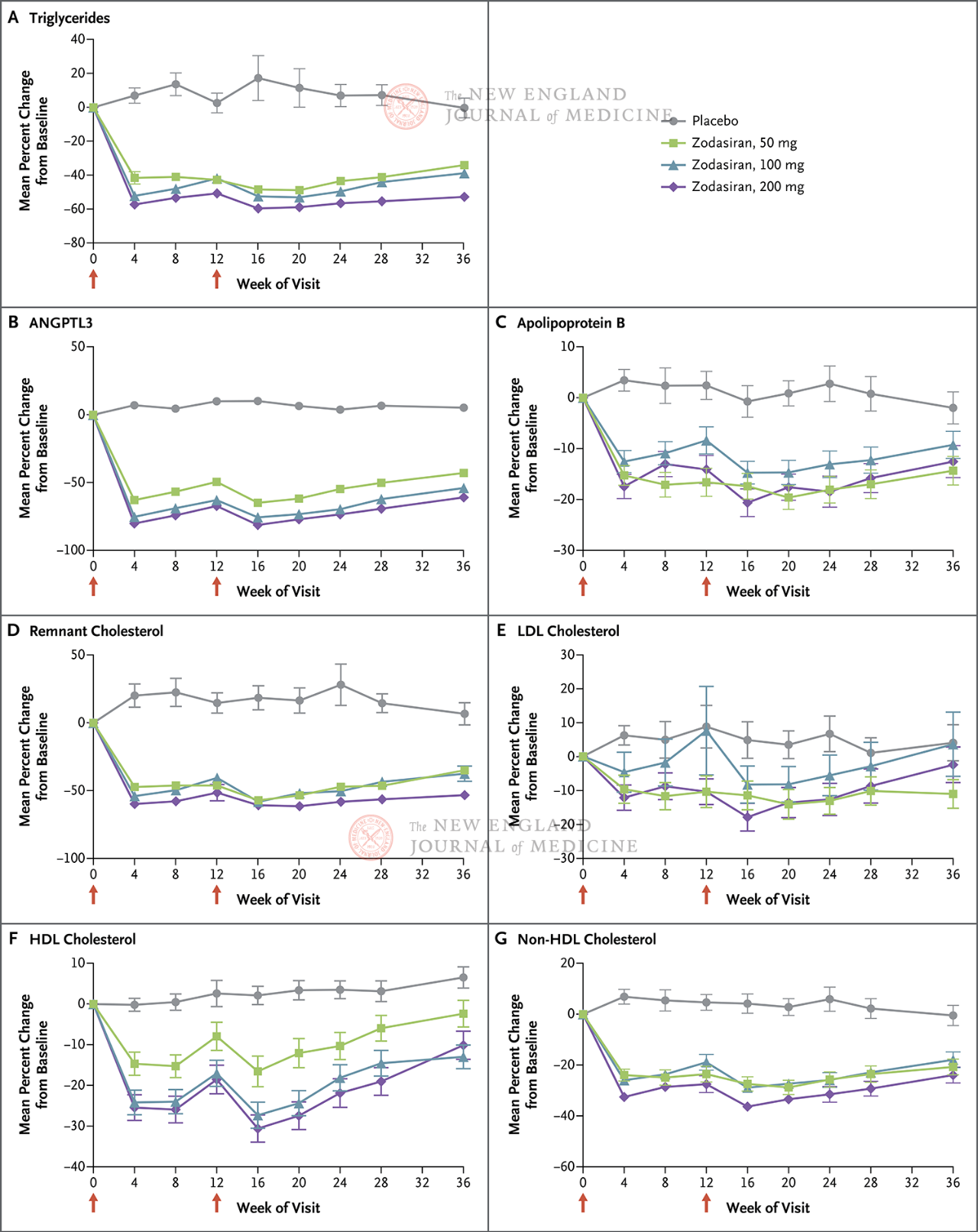
Первинною кінцевою точкою була відсоткова зміна рівня ТГ від початкового рівня до 24-го тижня. Дослідження показало, що до 24-го тижня рівні ТГ у групі зодасірану значно знизилися дозозалежним чином (рівні ТГ у кожній дозовій групі знизилися на 51, 57 та 63 відсоткові пункти відповідно порівняно з групами плацебо) (P < 0,001 для всіх порівнянь). ANGPTL3 також знизився на 54 відсоткові пункти, 70 відсоткових пунктів та 74 відсоткові пункти відповідно. Рівні не-ЛПВЩ знизилися на 29 відсоткових пунктів, 29 відсоткових пунктів та 36 відсоткових пунктів, рівні аполіпопротеїну B знизилися на 19 відсоткових пунктів, 15 відсоткових пунктів та 22 відсоткові пункти, а рівні ЛПНЩ знизилися на 16 відсоткових пунктів, 14 відсоткових пунктів та 20 відсоткових пунктів відповідно, і ці результати зберігалися до 36-го тижня. На 24-му тижні зодасіран
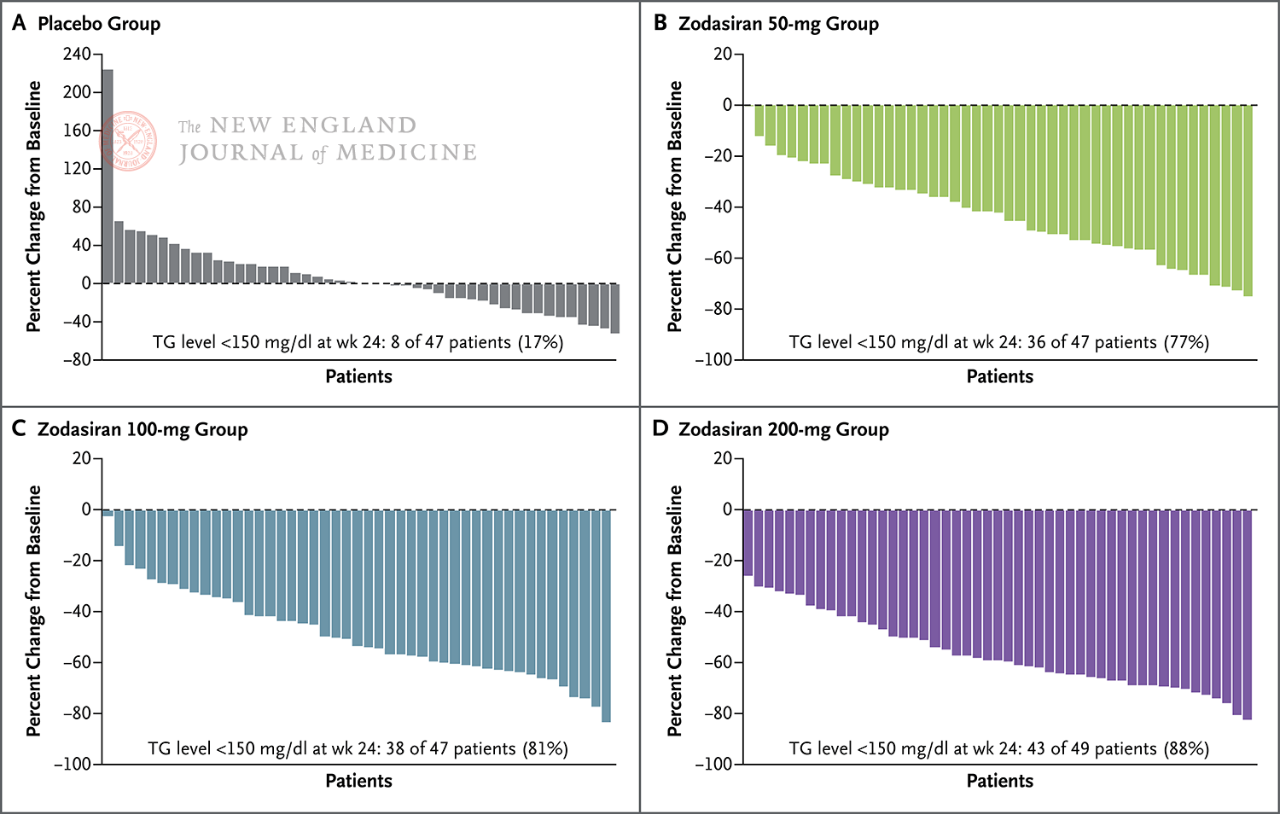
У 88% пацієнтів у групі, яка приймала 200 мг, рівень тригліцеридів натщесерце знизився до норми.
Червоні стрілки на 1-й та 12-й дні вказують на введення зодасирана або плацебо.
Рівень тригліцеридів натщесерце знизився до норми на 24-му тижні (150
мг/дл або менше)
Кожен стовпчик представляє одного пацієнта.
У дослідженні також було зазначено, що зотасіран був безпечним у всіх дозових групах, лише 2 пацієнти припинили дослідження через побічні ефекти (1 у групі плацебо та 1 у групі зотасірану 100 мг). Усі серйозні побічні ефекти в групі зотасірану відновилися до кінця дослідження, і в групі плацебо був один летальний випадок. Єдиним побічним ефектом, що викликав занепокоєння, було підвищення рівня HBA1c у групі зотасірану 200 мг порівняно з плацебо (середня зміна від початкового рівня до 24-го тижня [±SD], 0,38±0,66% проти -0,03±0,88% у пацієнтів з попереднім діабетом). Пацієнти без діабету становили 0,12±0,19% проти -0,03±0,19%).
Зокрема, майже всі пацієнти в дослідженні (96%) отримували статини (37% з яких були статинами у високих дозах), 1% отримували інгібітор пропротеїнперетворюючого ферменту субтилізину 9 (PCSK9i), а 21% отримували фібрати. Таким чином, додавання зодасірану до поточного звичайного режиму лікування все ще досягло значного ліпідознижувального ефекту, що забезпечує новий режим лікування змішаної гіперліпідемії в майбутньому.
На 24-му тижні максимальна доза зотасірану 200 мг у дослідженні знизила рівень залишкового холестерину на 34,4 мг/дл порівняно з плацебо. Виходячи з сучасних моделей, очікується, що це зниження зменшить основні побічні ефекти з боку серця на 20 відсотків. Зодасіран має потенціал для використання як монотерапія для всіх ліпопротеїнових компонентів для зниження ризику серцево-судинних подій у пацієнтів. Тому необхідні подальші дослідження, щоб визначити потенціал цього препарату у зниженні ризику атеросклеротичного захворювання.
У подвійному сліпому, рандомізованому, плацебо-контрольованому дослідженні MUIR фази 2b, опублікованому одночасно в NEJM, для лікування змішаної гіперліпідемії використовувався інший препарат на основі siRNA, плозасіран [2]. Плозасіран призначений для зниження експресії APOC3, гена, що кодує аполіпопротеїн C3 (APOC3), регулятор метаболізму тригліцеридів, у печінці, тим самим знижуючи рівень тригліцеридів та залишкового холестерину. Зниження рівня тригліцеридів та залишкового холестерину, що спостерігалося в дослідженні, було подібним до тих, що були виявлені в дослідженні ARCHES-2. Тому припускається, що у пацієнтів зі змішаною гіперліпідемією ці два препарати мають подібний ефект щодо зниження рівня ліпопротеїнів, багатих на тригліцериди, та залишкового холестерину.
Результати двох досліджень siRNA показують, що це дуже перспективний клас препаратів, який відкриє нові можливості для лікування змішаної гіперліпідемії та покращить серцево-судинні результати у пацієнтів.
Час публікації: 15 вересня 2024 р.